The Ikatan hidrogen adalah interaksi antara molekul yang serupa dengan interaksi Van der Waals dan berlaku di dalam tubuh manusia. Ikatan ini berperanan terutamanya berkaitan dengan ikatan peptida dan rantai asid amino dalam protein. Organisma tidak dapat dilaksanakan tanpa kemampuan untuk mengikat ikatan hidrogen kerana kekurangan asid amino penting.
Apakah ikatan hidrogen?

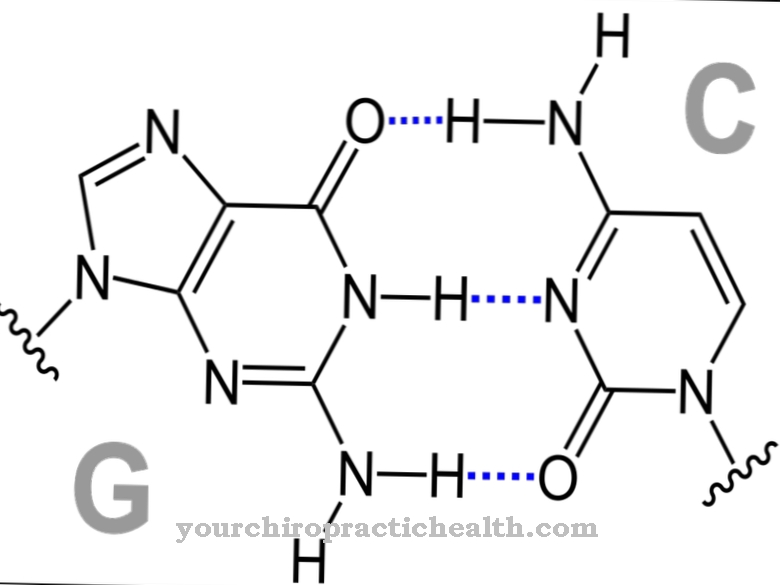
Ikatan hidrogen dipanggil Ikatan hidrogen atau Jambatan H disingkat. Ini adalah kesan kimia yang berkaitan dengan interaksi menarik atom hidrogen yang terikat secara kovalen dengan pasangan elektron bebas dari atom pengelompokan atom. Interaksi tersebut berdasarkan polaritas dan, yang dijelaskan dengan lebih tepat, terdiri antara atom hidrogen yang terpolarisasi positif dalam kumpulan amino atau hidroksil dan pasangan elektron tunggal dalam kumpulan berfungsi yang lain.
Interaksi itu berlaku hanya dalam keadaan tertentu. Satu syarat adalah sifat elektronegatif pasangan elektron bebas. Sifat ini mesti lebih kuat daripada sifat elektronegatif hidrogen untuk mewujudkan ikatan yang kuat. Oleh itu, atom hidrogen boleh terikat dengan kutub. Contohnya, atom bebas elektronegatif ialah nitrogen, oksigen dan fluorin.
Ikatan hidrogen adalah ikatan valensi sekunder, kekuatannya biasanya jauh lebih rendah daripada ikatan kovalen atau ikatan ionik. Molekul dalam ikatan hidrogen mempunyai titik lebur yang agak tinggi dan takat didih yang sama tinggi dengan jisim molarnya. Ikatan ini mempunyai kaitan perubatan terutamanya berkaitan dengan peptida dan asid nukleik dalam organisma.
Ikatan hidrogen adalah daya antara molekul. Tanpa keberadaannya, air tidak akan ada di berbagai keadaan agregat, tetapi akan menjadi gas.
Fungsi & tugas
Ikatan hidrogen hanya mempunyai interaksi yang lemah dan berlaku di antara dua zarah atau di dalam molekul. Dalam konteks ini, bentuk ikatan berperanan, misalnya, untuk pembentukan struktur tersier dalam protein. Dalam biokimia, struktur protein bermaksud tahap struktur protein atau peptida yang berbeza. Struktur bahan-bahan yang berlaku secara semula jadi ini dibahagikan secara hierarki menjadi struktur primer, struktur sekunder, struktur tersier dan struktur kuarter.
Urutan asid amino adalah struktur utama. Setiap kali protein disebutkan berkaitan dengan susunan spatialnya, konformasi protein dan fenomena perubahan konformasi sering disebut. Dalam konteks ini, perubahan konformasi sesuai dengan perubahan struktur spasial. Susunan protein berdasarkan ikatan peptida. Ikatan jenis ini selalu menghubungkan asid amino dengan cara yang sama.
Dalam sel, ikatan peptida dimediasi oleh ribosom. Setiap ikatan peptida sesuai dengan hubungan kumpulan karboksil satu asid amino dan kumpulan amino asid amino kedua, yang berkaitan dengan penghapusan air. Proses ini juga dikenali sebagai hidrolisis.
Dalam setiap ikatan peptida, ikatan tunggal menghubungkan kumpulan C = O dengan kumpulan NH. Atom nitrogen mempunyai satu elektron sepasang tunggal. Kerana elektronegativiti oksigen yang tinggi, pasangan bebas ini berada di bawah pengaruh penarikan elektron atom O2. Dengan cara ini, oksigen menarik sepasang elektron sepasang ke ikatan antara atom nitrogen dan atom karbon, dan ikatan peptida memperoleh watak ikatan berganda separa. Perwatakan ikatan berganda menghilangkan putaran bebas kumpulan NH dan C = O.
Atom oksigen dan atom hidrogen ikatan peptida adalah relevan untuk pembentukan struktur semua peptida dan protein tanpa kecuali. Dengan cara ini, dua asid amino boleh saling melekat. Selepas ikatan seperti itu, semua ikatan peptida dua rantai asid amino betul-betul bertentangan antara satu sama lain. Atom hidrogen dalam ikatan peptida relatif positif terpolarisasi jika dibandingkan dengan atom oksigen dalam ikatan peptida yang bertentangan langsung. Dengan cara ini, ikatan hidrogen membentuk dan menghubungkan dua rantai asid amino antara satu sama lain.
Semua asid amino dalam tubuh manusia adalah sebatian organik yang terdiri daripada sekurang-kurangnya satu kumpulan karboks dan satu kumpulan amino. Asid amino adalah komponen struktur penting dalam kehidupan manusia. Sebagai tambahan kepada asid α-amino protein, lebih daripada 400 asid amino bukan proteinogenik dengan fungsi biologi diketahui tidak dapat terbentuk tanpa ikatan hidrogen. Kekuatan seperti ikatan hidrogen menstabilkan struktur tersusun asid amino.
Anda boleh mendapatkan ubat anda di sini
➔ Ubat untuk kelemahan ototPenyakit & penyakit
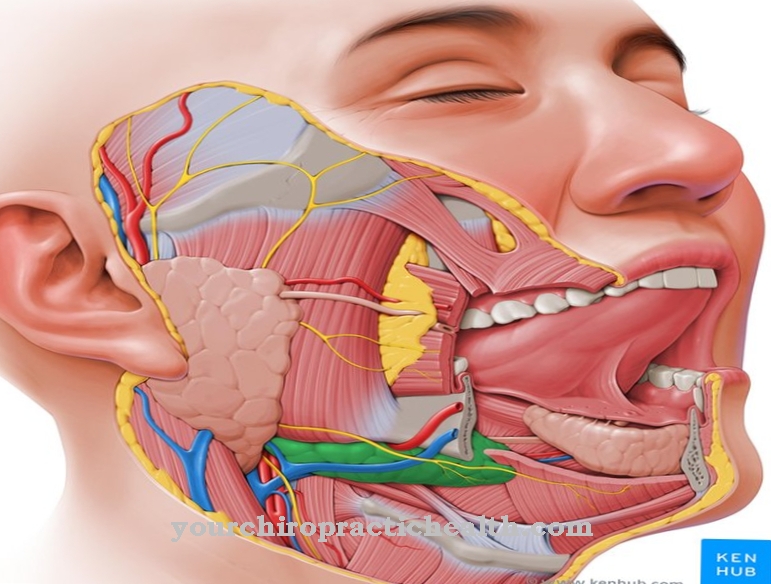
Sekiranya terdapat gangguan dalam pembentukan struktur spasial protein-energetik yang berfungsi, seseorang biasanya bercakap mengenai gangguan lipatan protein. Salah satu keadaan seperti penyakit Huntington. Gangguan genetik ini diwarisi sebagai sifat dominan autosomal dan disebabkan oleh mutasi genetik dalam kromosom 4. Mutasi tersebut menyebabkan ketidakstabilan produk gen. Penyakit ini adalah penyakit neurologi yang terutama berkaitan dengan hiperkinesis sukarela pada hujung dan muka yang jauh. Hiperkinesis berterusan menyebabkan ketegaran pada otot yang terjejas. Di samping itu, pesakit dengan penyakit ini mengalami peningkatan penggunaan tenaga.
Gejala patologi berkaitan dengan ikatan hidrogen atau struktur protein umum juga terdapat pada penyakit prion seperti penyakit lembu gila. Menurut hipotesis yang paling popular, BSE memulakan salah protein. Protein yang salah dilipat ini tidak dapat dipecah oleh proses fisiologi dan oleh itu terkumpul di dalam tisu, terutama di sistem saraf pusat. Hasilnya adalah degenerasi sel-sel saraf.
Juga dalam hubungan sebab akibat penyakit Alzheimer, struktur protein dibincangkan. Penyakit yang disebutkan tidak mempengaruhi ikatan hidrogen secara langsung, tetapi berkaitan dengan struktur spasial protein, yang mana ikatan hidrogen memberikan sumbangan yang besar.
Organisma dengan ketidakupayaan mutlak untuk ikatan hidrogen tidak dapat dilaksanakan. Mutasi yang menyebabkan ini akan menyebabkan pengguguran pada awal kehamilan.








.jpg)





-eisenmangelanmie.jpg)